В периодическую таблицу элементов придётся внести некоторые изменения
Друзья, с момента основания проекта прошло уже 20 лет и мы рады сообщать вам, что сайт, наконец, переехали на новую платформу.
Какое-то время продолжим трудится на общее благо по адресу
На новой платформе мы уделили особое внимание удобству поиска материалов.
Особенно рекомендуем познакомиться с работой рубрикатора.
Спасибо, ждём вас на N-N-N.ru
Специальная комиссия Международного союза теоретической и прикладной химии (IUPAC) опубликовала обновлённую таблицу атомных весов, в которой вес 10 элементов впервые указан в виде интервалов значений.
Атомный вес, приведённый в обычной периодической таблице элементов, мы привыкли считать константой. Это справедливо, но только в случае элементов с одним стабильным изотопом (фтора, алюминия, натрия и других); если таких изотопов два или больше, необходимо вычислять средневзвешенный атомный вес с учётом их природной распространённости.
Указанные в таблице результаты вычислений приходилось довольно часто обновлять. Многих вводил в заблуждение сам вид записи: смотря, к примеру, на атомный вес водорода, равный 1,00794(7), они удивлялись, почему «погрешность измерения» (которая на самом деле не имеет к измерениям никакого отношения и введена для того, чтобы охватить различные опубликованные значения) так велика.
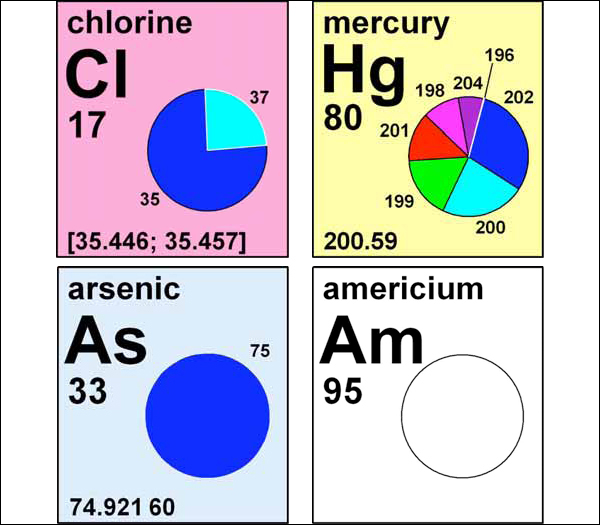 Рис. 1. Примеры графических изображений для периодической таблицы, на которых круговыми диаграммами отмечена распространённость изотопов. Атомный вес хлора и ртути не является константой, но у первого элемента указывается в виде интервала, а у второго — единичным значением. У мышьяка есть только один стабильный изотоп, поэтому его атомный вес можно считать константой. Стабильных изотопов америция не существует, поэтому значение атомного веса ему не присваивается. (Иллюстрация из журнала Chemistry International).
Рис. 1. Примеры графических изображений для периодической таблицы, на которых круговыми диаграммами отмечена распространённость изотопов. Атомный вес хлора и ртути не является константой, но у первого элемента указывается в виде интервала, а у второго — единичным значением. У мышьяка есть только один стабильный изотоп, поэтому его атомный вес можно считать константой. Стабильных изотопов америция не существует, поэтому значение атомного веса ему не присваивается. (Иллюстрация из журнала Chemistry International).
Теперь стандартная форма записи изменяется, и атомный вес водорода будет обозначаться интервалом [1,00784; 1,00811]. Аналогичным образом модифицируются значения для лития, бора, углерода, азота, кислорода, кремния, серы, хлора и таллия. Кроме того, в новой таблице представлен уточнённый атомный вес германия, который теперь равняется 72,64(1).
Как отмечает Майкл Визер (Michael Wieser) из Университета Калгари, секретарь комиссии IUPAC по атомным массам и распространенности изотопов, изучающей распространенность различных изотопов в земной коре и уточняющей значения атомных масс, почти полтора столетия мы пользовались стандартным набором значений атомных весов, определённых еще до таблицы Менделеева или скорректированных при ее создании. Однако аналитические технологии не стоят на месте, и во второй половине ХХ века стало ясно, что атомная масса не является статической для всей земной коры величиной, а зависит зачастую от места извлечения того или иного элемента.
Современные аналитические технологии могут осуществлять точные изменения атомных масс многих элементов, при этом незначительные изменения в значениях атомной массы очень часто могут оказаться важными как для решения исследовательских задач, так и на практике. Например, точное определение распространенности изотопов углерода в образце может использоваться для определения качества пищи или особенностей ее происхождения. Изотопное распределение азота, хлора и ряда других элементов важно для отслеживания перемещения загрязняющих веществ в гидросфере и грунтовых водах. При проведении допинг-контроля различия в изотопном составе могут также оказаться полезными – распределение изотопов в тестостероне, вырабатывающимся организмом человека и фармацевтическом тестостероне различно.
Чиновники IUPAC планируют активно продвигать нововведения в наступающем году, который, напомним, объявлен Международным годом химии.
Атомные массы элементов, встречающихся в земной коре в виде только одного стабильного изотопа, не различаются в зависимости от нахождения их в земной коре. Так, например, атомные массы фтора, алюминия, натрия и золота постоянны и определенны с точностью до шести цифр после запятой.
Как отмечает заместитель директора IUPAC Фабиен Мейерс (Fabienne Meyers), хотя новая система задания атомных масс в виде интервалов несет существенные преимущества в плане понимания химии и практического применения, он осознает, с какими трудностями столкнутся преподаватели химии и учащиеся, которым придется выбирать единственное значение атомной массы из интервала для применения в химических расчетах и решении задач. Он добавляет, что надеется на то, что преподаватели химии смогут преодолеть эти трудности, привить молодому поколению интерес к химии и подготовить новых исследователей. Фундаментальные изменения в способе представления атомных весов является результатом работ, проводившихся под эгидой IUPAC с 1985 по 2010 год.
Свежая таблица атомных весов будет опубликована в журнале Pure and Applied Chemistry. Пояснения к решению IUPAC можно найти в другой статье, которая появится в мартовском номере журнала Chemistry International.
- Источник(и):
-
3. chemport.ru
- Войдите на сайт для отправки комментариев
 Сайт о нанотехнологиях #1 в России
Сайт о нанотехнологиях #1 в России