Разработана уникальная гибридная молекула для лечения остеопороза стволовыми клетками
Друзья, с момента основания проекта прошло уже 20 лет и мы рады сообщать вам, что сайт, наконец, переехали на новую платформу.
Какое-то время продолжим трудится на общее благо по адресу
На новой платформе мы уделили особое внимание удобству поиска материалов.
Особенно рекомендуем познакомиться с работой рубрикатора.
Спасибо, ждём вас на N-N-N.ru
Группа исследователей под руководством ученых из Калифорнийского университета в Дэвисе (University of California – Davis) разработала новый метод стимуляции роста костей с помощью молекулы, которая при введении в кровь направляет к их поверхности стволовые клетки костного мозга.
Достигнув поверхности кости, стволовые клетки дифференцируются в клетки, образующие кость, и синтезируют белки, усиливающие ее рост. В исследовании, опубликованном в журнале Nature Medicine, ученые использовали мышиную модель остеопороза, чтобы продемонстрировать уникальный подход к лечению, повышающий плотность костной ткани и предотвращающий потерю костной массы, связанные со старением и дефицитом в организме женских половых гормонов эстрогенов.
«Даже у пожилых людей много стволовых клеток, но они не охотно мигрируют к костям», – говорит ведущий автор исследования Вэй Яо (Wei Yao). «Разработка молекулы, которая связывается со стволовыми клетками и направляет их к нужной нам цели, – это настоящий прорыв».
Ученые изучают стволовые клетки как возможный метод лечения широкого спектра болезней и травм – от поражения периферических артерий и макулярной дегенерации до болезней крови и органов и кожных ран. Однако заставить стволовые клетки мигрировать к поверхности костей и стимулировать их рост долго оставалось одной из недостижимых целей регенеративной медицины.
Американские ученые использовали уникальную гибридную молекулу, LLP2A-алендронат, разработанную группой во главе с Китом Ламом (Kit Lam), профессором и заведующим кафедрой биохимии и молекулярной медицины UC Davis. Гибридная молекула состоит из двух частей: синтетической молекулы-лиганда LLP2A, связывающейся с мезенхимальными стволовыми клетками в костном мозге, и второй части, состоящей из «самонаводящегося» препарата для лечения костей – алендроната. После введения в кровь гибридная молекула связывается с мезенхимальными стволовыми клетками в костном мозге и направляет эти клетки к поверхности костей, где они выполняют свои естественные функции – образование и восстановление костной ткани.
 Профессор биохимии и молекулярной
Профессор биохимии и молекулярной
медицины Кит Лам (Kit Lam).
(Фото ucdmc.ucdavis.edu)
«Наше исследование подтверждает, что молекулы, связывающиеся со стволовыми клетками, могут быть использованы для их направления к органам животного, нуждающимся в лечении», – комментирует работу профессор Лам. «Это очень важный шаг к тому, чтобы сделать этот тип лечения стволовыми клетками реальностью».
Костная масса и прочность бедренной кости и позвоночника мышей увеличилась через двенадцать недель после введения им гибридных молекул. Положительные процессы в костях протекали как у мышей в возрасте активной потери костной массы, так и у животных с моделью менопаузы.
Алендронат, известный также под торговой маркой Фосамакс (Fosamax), обычно назначается женщинам с остеопорозом, чтобы снизить риск переломов. Ученые включили алендронат в гибридную молекулу, потому что, попадая в кровь, она направляется прямо к поверхности костей и замедляет скорость их разрушения. По словам соавтора исследования Нэнси Лейн (Nancy Lane), доза алендроната в гибридном соединении низка и вряд ли способна снизить его терапевтический эффект.
«Впервые мы, возможно, нашли потенциальный способ направить собственные стволовые клетки пациента к поверхности кости, где они могут ее восстановить», – говорит профессор медицины и ревматологии Лейн, специалист по остеопорозу. «Этот метод может совершить революцию в терапии остеопороза, а также других заболеваний, требующих образования новой костной ткани».
Остеопороз является одной из основных проблем общественного здравоохранения, учитывая тот факт, что только в США им страдают 44 миллиона американок. Несмотря на доступность эффективных лекарственных препаратов, способных снизить риск переломов, в том числе алендроната, их назначение ограничивается потенциально опасными последствиями длительного применения.
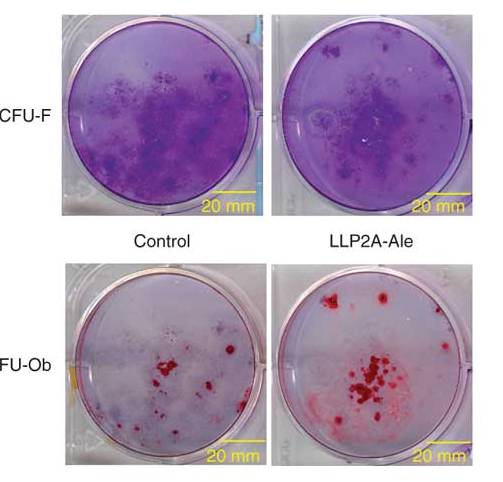 Старение уменьшает количество мезенхимальных стволовых клеток (МСК), дифференцирующихся в костном мозге в остеобласты, что приводит к нарушению остеогенеза. Стимуляция дифференцировки МСК в остеогенном направлении могла бы стать надежным способом регенерации кости. Ученые разработали метод, позволяющий направить МСК к поверхности кости путем присоединения синтетического лиганда-пептидомиметика (LLP2A) с высоким сродством и специфичностью к белку интегрину α4β1 на поверхности МСК к бисфосфонату (алендронату, Ale) с высокой аффинностью к костной ткани. Гибридная молекула LLP2A-Ale индуцирует миграцию МСК и остеогенную дифференцировку in vitro. Одно внутривенное введение LLP2A-Ale усиливает образование губчатой кости и костной массы как в ксенотранспланционных исследованиях, так и у иммунокомпетентных мышей. Кроме того, LLP2A-Ale предотвращает возрастную и вызванную дефицитом эстрогенов потерю трабекулярной костной массы. Эти результаты являются доказательством принципа, что LLP2A-Ale может направлять МСК к кости и стимулировать образование новой костной ткани и увеличение прочности костей. На фото стволовые клетки костного мозга, выращенные в остеогенной среде (контроль) и с LLP2A-Ale. Колониеобразующие фибробластические клетки (CFU-F) окрашены фиолетовым, колониеобразующие остеобласты (CFU-Ob), субпопуляция CFU-F, – красным. (Фото: nature.com)
Старение уменьшает количество мезенхимальных стволовых клеток (МСК), дифференцирующихся в костном мозге в остеобласты, что приводит к нарушению остеогенеза. Стимуляция дифференцировки МСК в остеогенном направлении могла бы стать надежным способом регенерации кости. Ученые разработали метод, позволяющий направить МСК к поверхности кости путем присоединения синтетического лиганда-пептидомиметика (LLP2A) с высоким сродством и специфичностью к белку интегрину α4β1 на поверхности МСК к бисфосфонату (алендронату, Ale) с высокой аффинностью к костной ткани. Гибридная молекула LLP2A-Ale индуцирует миграцию МСК и остеогенную дифференцировку in vitro. Одно внутривенное введение LLP2A-Ale усиливает образование губчатой кости и костной массы как в ксенотранспланционных исследованиях, так и у иммунокомпетентных мышей. Кроме того, LLP2A-Ale предотвращает возрастную и вызванную дефицитом эстрогенов потерю трабекулярной костной массы. Эти результаты являются доказательством принципа, что LLP2A-Ale может направлять МСК к кости и стимулировать образование новой костной ткани и увеличение прочности костей. На фото стволовые клетки костного мозга, выращенные в остеогенной среде (контроль) и с LLP2A-Ale. Колониеобразующие фибробластические клетки (CFU-F) окрашены фиолетовым, колониеобразующие остеобласты (CFU-Ob), субпопуляция CFU-F, – красным. (Фото: nature.com)
Основными причинами развития остеопороза у женщин являются дефицит эстрогенов, старение и избыток стероидов в результате лечения хронических воспалительных заболеваний, таких как ревматоидный артрит. Как правило, остеопороз, вызванный этими метаболическими заболеваниями, развивается в результате изменений в цикле ремоделирования костной ткани, которые ослабляют архитектуру кости и увеличивают риск переломов.
Ученые отмечают, что использование этого метода регенеративной медицины не ограничивается терапией остеопороза. Он может оказаться бесценным и при других нарушениях и заболеваниях, когда необходимо усилить восстановление костной ткани, например, при переломах, костных инфекциях или раке.
По мнению одного из участников исследования директора Института регенеративной терапии (Institute for Regenerative Cures) при UC Davis Йены Нолты (Jan Nolta), полученные результаты являются весьма перспективными с точки зрения их клинического применения. «Мы показали эффективность этого потенциального метода терапии на грызунах, и теперь наша цель – перейти к его клиническим испытаниям».
Аннотация к статье
Directing mesenchymal stem cells to bone to augment bone formation and increase bone mass
- Войдите на сайт для отправки комментариев
 Сайт о нанотехнологиях #1 в России
Сайт о нанотехнологиях #1 в России