Генно-инженерные Т-лимфоциты атакуют рак яичников
Друзья, с момента основания проекта прошло уже 20 лет и мы рады сообщать вам, что сайт, наконец, переехали на новую платформу.
Какое-то время продолжим трудится на общее благо по адресу
На новой платформе мы уделили особое внимание удобству поиска материалов.
Особенно рекомендуем познакомиться с работой рубрикатора.
Спасибо, ждём вас на N-N-N.ru
В последнем номере журнала Cancer Research научный сотрудник кафедры патологии и лабораторной медицины и акушерства и гинекологии Школы медицины Перельмана при Университете Пенсильвании (University of Pennsylvania) Дэниэл Пауэлл-младший (Daniel J. Powell, Jr.) сообщает о значительном успехе в иммунотерапии рака: биоинженерные человеческие Т-клетки могут излечивать человеческий рак яичников у иммунодефицитных мышей.
Рак яичников – заболевание женской репродуктивной системы с наибольшей смертностью: пятилетняя выживаемость женщин с поздно диагностированным заболеванием составляет лишь 20%.
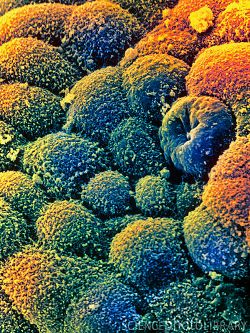 Клетки рака яичников.
Клетки рака яичников.
Самый распространенный тип рака яичников –
карцинома, развивающаяся из эпителиальных
клеток. (СЭМ). (Фото: Science Photo Library)
В проведенных ранее клинических исследованиях первое поколение инженерных Т-клеток не сокращало размер опухолей у женщин с раком яичников, так как Т-клетки быстро погибали в организме пациенток. Технология второго поколения, разработанная в данном исследовании, преодолела многие недостатки подхода, использованного для создания клеток первого поколения. Биоинженерные Т-клетки второго поколения сокращают размер опухолей.
Почти для всех случаев рака яичников (90%) характерна экспрессия мембранного белка – рецептора фолиевой кислоты альфа. Рецепторы фолиевой кислоты альфа имеют высокое сродство к фолиевой кислоте, витамину, способствующему активному росту опухоли. Эти рецепторы представляют собой «ахиллесову пяту» раковых клеток, которую ученые используют в качестве мишени для их уничтожения.
Инженерные Т-клетки первого поколения, экспрессирующие фрагмент антитела, специфичный для белка рецептора фолиевой кислоты альфа, показывали достаточно высокую противоопухолевую активность по отношению к эпителиальным ракам в лаборатории. Но их клинические испытания закончились неудачей из-за неспособности клеток связываться с опухолями и сохраняться в организме человека. Модифицированные Т-клетки, используемые в новом исследовании, экспрессируют инженерный белок слияния, называемый химерным антигенным рецептором, который сочетает в себе специфичность антитела с сигнальными компонентами двух различных белков Т-клеток, стимулирующих распознавание иммунной системой клеток рака яичников. Эти добавленные части сигнальных белков дают инженерным Т-клеткам дополнительные сигналы к выживанию, необходимые им для выполнения своей функции.
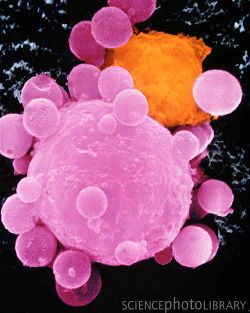 Лимфоцит (оранжевый)
Лимфоцит (оранжевый)
атакует раковую клетку. (СЭМ).
(Фото: Science Photo Library)
Модифицированные Т-клетки сконструированы таким образом, что могут выживать, размножаться, распознавать и убивать опухоли яичников. В течение двух недель они культивируются в лаборатории, а затем проходят проверку на реактивность в присутствии клеток человеческого рака яичников. Чтобы убедиться в их эффективности, ученые оценивают и выработку ими цитокинов, Выработка цитокинов – признак воспаления, сопровождающего и подтверждающего гибель раковых клеток.
Инженерные Т-клетки второго поколения превосходят клетки первого поколения во многих отношениях. Они более устойчивы к индуцированной раком клеточной смерти: раковые клетки убивают меньшее их количество. Для них характерна лучшая выживаемость и способность к размножению, поэтому в экспериментах in vivo и в мышиной модели заболевания их количество со временем увеличивается.
Начало клинических испытаний генетически модифицированных Т-клеток ожидается в течение ближайших месяцев. К ним будет привлечено до 21 пациентки с прогрессирующим рецидивирующим раком яичников, экспрессирующим рецепторы фолиевой кислоты альфа.
 Дэниэл Пауэлл-младший
Дэниэл Пауэлл-младший
(Daniel J. Powell, Jr.)
(Фото: med.upenn.edu)
«Эта технология представляет собой многообещающее достижение в лечении женщин с раком яичников», – говорит Пауэлл. «Но мы будем неустанно работать, чтобы усовершенствовать этот подход, используя другие костимуляторные компоненты и подобные антителам белки, чтобы сделать его самым мощным и безопасным подходом для лечения как можно большего числа женщин с этим ужасным заболеванием».
Аннотация к статье
- Источник(и):
- Войдите на сайт для отправки комментариев
 Сайт о нанотехнологиях #1 в России
Сайт о нанотехнологиях #1 в России