ДНК-оригами сделает токсичный противораковый препарат безопасным
Друзья, с момента основания проекта прошло уже 20 лет и мы рады сообщать вам, что сайт, наконец, переехали на новую платформу.
Какое-то время продолжим трудится на общее благо по адресу
На новой платформе мы уделили особое внимание удобству поиска материалов.
Особенно рекомендуем познакомиться с работой рубрикатора.
Спасибо, ждём вас на N-N-N.ru
Исследователи из Каролинского института (Швеция) продемонстрировали, как с помощью ДНК-оригами можно усилить эффект действия цитостатиков в противораковой терапии. Используя современную нанотехнологию, учёные получили возможность доставлять лекарственный препарат в опухоль, не затрагивая окружающих здоровых тканей.
Доксорубицин довольно давно применяется в противораковой терапии в качестве эффективного цитостатика, вещества, препятствующего делению клеток. Увы, его использование сильно ограничено неприятными побочными эффектами, при которых в первую очередь страдает сердце больного (препарат токсичен для клеток сердечной мышцы и легко может вызвать её остановку).
Именно поэтому вопрос направленной доставки активного вещества прямо к клеткам опухоли стоит особенно остро. Одно из возможных решений, на которое возлагается больше всего надежд, — применение наночастиц, загруженных лекарством.
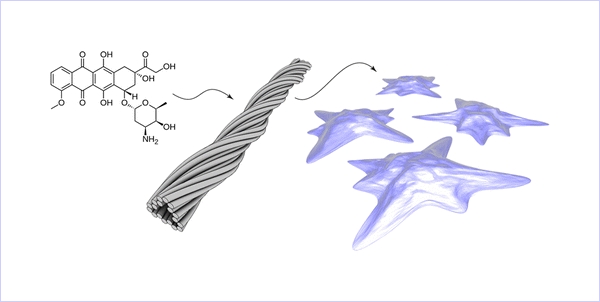 Рис. 1. Молекулу доксорубицина (слева) помещают внутрь ДНК-оригами с поверхностью, модифицированной для селективного взаимодействия с раковыми клетками (справа). (Иллюстрация ACS).
Рис. 1. Молекулу доксорубицина (слева) помещают внутрь ДНК-оригами с поверхностью, модифицированной для селективного взаимодействия с раковыми клетками (справа). (Иллюстрация ACS).
В исследовании, результаты которого представлены в журнале ACS Nano, шведские учёные показали, что
в качестве носителя доксорубицина может использоваться ДНК-оригами.
ДНК-оригами — относительно новая техника построения объёмных наноструктур из молекул ДНК, наследственного материала, присутствующего в ядрах клеток. При её применении становится возможным изготавливать довольно сложные наноструктуры с поверхностями, к которым можно привязать самые разные молекулы и протеины (что очень непросто в случае с неорганическими наночастицами).
Итак, доксорубицин был упакован внутрь оригами из «недокрученных» двойных спиралей ДНК (иными словами, из молекул с пониженной степенью скручивания), что дало возможность замедлить скорость выхода препарата и, следовательно, повысить его эффективность при действии на клетки опухоли.
При этом используемые концентрации лекарства были чуть ли не рекордно низкими.
В чём тут причина? При более низкой степени скручивания ДНК появляется больше мест, способных удерживать молекулу доксорубицина, что в целом снижает скорость выхода вещества наружу (кинетический контроль). Ещё одно достоинство ДНК-оригами заключается в том, что его поверхность очень легко модифицировать под конкретную белковую мишень, обеспечив тем самым высочайшую степень селективности, при которой здоровые клетки могут чувствовать себя в полной безопасности.
- Источник(и):
-
3. phys.org
- Войдите на сайт для отправки комментариев
 Сайт о нанотехнологиях #1 в России
Сайт о нанотехнологиях #1 в России