«Умная» нановолоконная сеть борется с раком теплом и лекарствами
Друзья, с момента основания проекта прошло уже 20 лет и мы рады сообщать вам, что сайт, наконец, переехали на новую платформу.
Какое-то время продолжим трудится на общее благо по адресу
На новой платформе мы уделили особое внимание удобству поиска материалов.
Особенно рекомендуем познакомиться с работой рубрикатора.
Спасибо, ждём вас на N-N-N.ru
Исследовательская группа из MANA (International Center for Materials Nanoarchitectonics), Япония, разработала сеть из нановолокон, способную одновременно реализовывать как термотерапию (гипертермию), так и химиотерапию (лечение противоопухолевыми препаратами) раковых новообразований. Ученым удалось эффективно индуцировать естественную смерть (апоптоз) клеток рака эпителия.
Плоскоклеточная карцинома – злокачественная опухоль эпителиальной ткани. Считается, что плоскоклеточный рак составляют более 90% всех раковых опухолей пищевода, более 80% рака шейки матки и более 30% рака легких.
В последние годы к традиционным методам лечения рака – хирургии, облучению и химиотерапии – добавилась термотерапия. Известно, что по сравнению с нормальными раковые клетки более чувствительны к повышенной температуре, что позволяет добиться их гибели воздействием теплом. Кроме того, установлено, что при использовании в сочетании с химиотерапией термотерапия усиливает действие противоопухолевых препаратов. Однако, когда в реальных клинических условиях пациенту назначаются как медикаментозное лечение, так и термотерапия, эти методы приходится применять независимо друг от друга. В результате на сегодня точный контроль над одновременным лечением одной опухоли двумя разными методами остается трудно реализуемой задачей.
Группа во главе с доктором Мицухиро Эбара (Mitsuhiro Ebara) решила эту проблему, разработав метод одновременного применения термо- и химиотерапии для лечения злокачественных опухолей эпителия. Ученые разработали сетчатый материал, наносимый непосредственно на пораженный участок, представляющий собой гибрид, состоящий из термочувствительного полимера, магнитных наночастиц и противоопухолевого препарата.
Недавно разработанные методы магнитной термотерапии, в которых обладающие магнитными свойствами наночастицы вводятся непосредственно в организм, вызывают озабоченность в связи с безопасностью самих наночастиц. Кроме того, введенными в организм наночастицами трудно управлять. Разработанная нановолоконная сеть проста в управлении и может быть использована в эндоскопической хирургии. Более того, поскольку содержащиеся в волокнах магнитные частицы стабильны и прочно удерживаются полимерной сетью, их попадание в организм сводится к минимуму, и новый метод, как полагают, обеспечивают более высокую безопасность.
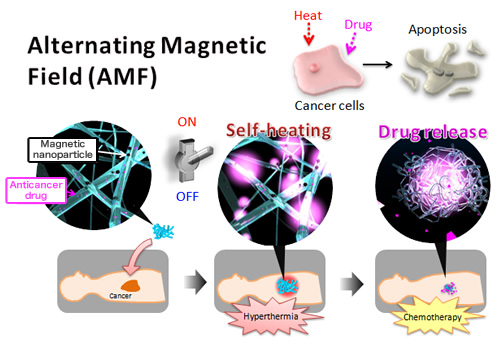 Концепция дизайна «умной» нановолоконной системы для гипертермии с использованием магнитных наночастиц (MNPs), диспергированных в термочувствительных
Концепция дизайна «умной» нановолоконной системы для гипертермии с использованием магнитных наночастиц (MNPs), диспергированных в термочувствительных
полимерах. Помимо MNPs в химически сшитые нановолокна включен противоопухолевый препарат (доксорубицин, DOX). Включение («ON») переменного магнитного поля (AMF)
активирует MNPs в нановолокнах. Под воздействием генерируемого MNPs тепла полимерные сети нановолокон сжимаются, позволяя осуществлять «ON-OFF» контроль
над высвобождением доксорубицина. Генерируемое тепло и высвободившийся DOX индуцируют апоптоз раковых клеток за счет эффекта гипертермии и химиотерапии, соответственно.
(Рис. National Institute for Materials Science)
Так как нановолоконная сеть содержит магнитные наночастицы – самонагревающееся вещество, – волокна можно нагревать путем приложения переменного магнитного поля. Кроме того, в ответ на тепло, генерируемое магнитными наночастицами, термочувствительный полимер сжимается, что вызывает высвобождение содержащегося в нановолоконной сети противоопухолевого препарата. При проверке противоопухолевой активности этой сети на клеточной линии человеческой меланомы было установлено, что путем приложения переменного магнитного поля можно эффективно осуществлять «ON-OFF» контроль над индуцированием апоптоза раковых клеток.
Поскольку вновь разработанная нановолоконная сеть позволяет осуществлять одновременное «ON-OFF» управление нагревом пораженной ткани и высвобождением лекарств с помощью простого внешнего стимула, этот подход является важным шагом вперед в развитии следующего поколения терапевтических материалов для медицины 21-го века.
Оригинальная статья A Smart Hyperthermia Nanofiber with Switchable Drug Release for Inducing Cancer Apoptosis опубликована в журнале Advanced Functional Materials.
- Источник(и):
- Войдите на сайт для отправки комментариев
 Сайт о нанотехнологиях #1 в России
Сайт о нанотехнологиях #1 в России