Химики получили водород на катоде и аноде одновременно
Друзья, с момента основания проекта прошло уже 20 лет и мы рады сообщать вам, что сайт, наконец, переехали на новую платформу.
Какое-то время продолжим трудится на общее благо по адресу
На новой платформе мы уделили особое внимание удобству поиска материалов.
Особенно рекомендуем познакомиться с работой рубрикатора.
Спасибо, ждём вас на N-N-N.ru
Ученые из США и Китая разработали систему электролиза, в которой на аноде и катоде выделялся водород. При этом протекало две реакции: окисление природного альдегида и восстановление воды. Такая система позволила получать водород при низком напряжении в цепи и небольшом потреблении энергии.
Исследование опубликовано в журнале Nature Catalysis.
95 процентов всего производимого водорода получают риформингом ископаемого топлива — дешевым, но вредным для окружающей среды процессом. В качестве альтернативы ученые долгое время предлагают электролиз воды, однако из-за высокого напряжения, требуемого для протекания реакции окисления, получать водород электролизом оказывается слишком дорого.
Еще одна проблема, из-за которой электролиз воды трудно применять в промышленности, заключается в следующем: в результате реакции на аноде выделяется водород, а на катоде — кислород, которые вместе дают очень взрывоопасную смесь. Из-за этого приходится разделять анодное и катодное пространства, а также тщательно контролировать состав получаемого газа. Кроме того, образующиеся в процессе радикальные частицы могут разрушать мембраны электролизера.
Химики под руководством Дуаня Сянфэня (Duan Xiangfeng) из Калифорнийского университета решили разработать метод электролитического получения водорода из дешевого органического исходного и воды. При этом их целью было провести электролиз при низком напряжении и без выделения побочных газообразных продуктов.
Химикам было известно, что альдегиды можно электрохимически окислять до карбоновых кислот в присутствии металлических катализаторов, при этом на поверхности металла адсорбируются атомы водорода, которые затем окисляются с образованием воды. Исходя из этого, авторы статьи предположили, что можно провести процесс, при котором адсорбированные атомы водорода будут объединяться с образованием молекулярного водорода, а не окисляться.
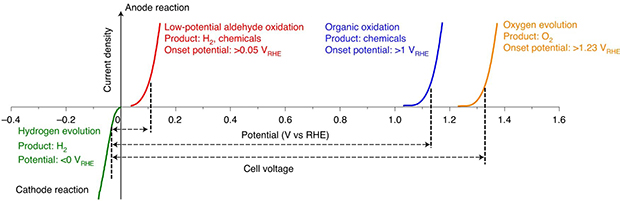 Значения напряжения, требуемые для электролиза воды и окисления альдегидов / D. Xiangfeng et al. / Nature Catalysis, 2021
Значения напряжения, требуемые для электролиза воды и окисления альдегидов / D. Xiangfeng et al. / Nature Catalysis, 2021
Для исследования реакции окисления химики выбрали альдегид гидроксиметилфурфураль — он встречается в природе и легко получается из сахаров. А в качестве катализатора ученые решили использовать металлическую медь с большой площадью поверхности, которую они предварительно получали электрохимическим восстановлением оксида меди Cu2O. Ученым удалось установить, что при проведении реакции анодного окисления ток в цепи возникает уже при напряжении в 0,05 Вольт, а затем повышается, достигая максимума около 0,4 Вольт. Масс-спектрометрический анализ показал, что продукты реакции — газообразный водород и соответствующая карбоновая кислота.
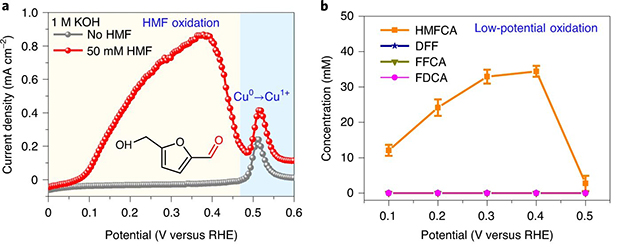 a) Зависимость потенциала от плотности тока. Первый пик отвечает окислению альдегида, а второй — окислению медного катализатора. b) Концентрация получившейся кислоты в зависимости от напряжения в цепи (желтая линия) / D. Xiangfeng et al. / Nature Catalysis, 2021
a) Зависимость потенциала от плотности тока. Первый пик отвечает окислению альдегида, а второй — окислению медного катализатора. b) Концентрация получившейся кислоты в зависимости от напряжения в цепи (желтая линия) / D. Xiangfeng et al. / Nature Catalysis, 2021
Чтобы получить еще больше водорода, химики попробовали объединить процесс окисления альдегида на аноде и реакцию выделения водорода из воды на катоде. В качестве анода они использовали металлическую медь, а в качестве катода выбрали платину на угле. Реакция началась уже при напряжении менее 0,1 Вольта, а плотность тока достигла 100 миллиампер на квадратный сантиметр при напряжении 0,27 Вольта.
В результате химикам удалось разработать эффективный процесс получения водорода. Рассчитанный выход по току составил 100 процентов и для анодного, и для катодного процесса (то есть на каждый прошедший через цепь электрон выделялась одна молекула водорода). При одинаковой плотности тока новый процесс позволил получать в два раза больше водорода, чем классический электролиз воды, а потребление энергии оказалось меньше примерно в 14 раз.
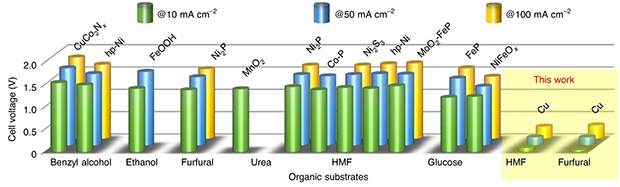 Сравнение эффективности разных органических субстратов в реакции получения водорода. По вертикальной оси отложено требуемое значение напряжения / D. Xiangfeng et al. / Nature Catalysis, 2021
Сравнение эффективности разных органических субстратов в реакции получения водорода. По вертикальной оси отложено требуемое значение напряжения / D. Xiangfeng et al. / Nature Catalysis, 2021
- Источник(и):
- Войдите на сайт для отправки комментариев
 Сайт о нанотехнологиях #1 в России
Сайт о нанотехнологиях #1 в России